Onlangs heeft de CieBOM voor een derde PARP remmer in de onderhoudsbehandeling van recidief platina-gevoelig ovariumcarcinoom een positief advies gegeven, voor rucaparib (Rubraca®).1 In de pivotale ARIEL3 studie zijn diverse patiënten opgenomen: BRCA mutatiedraagsters en non-BRCA gemuteerde patiënten (de HRD positieve groep en de algehele populatie), en mét of zonder restziekte.
De PFS werd geëvalueerd in de verschillende gecombineerde cohorten met een focus op de ‘Intention-To-Treat’ populatie (IIT) waarbij data van alle patiënten zijn verzameld, welke een PFS liet zien van 10,8 maanden en een vermindering van het risico op een recidief van 64% (HR: 0,36). De resultaten van de overige onderzochte studie cohorten waren: BRCA mutatiedraagsters: PFS 16,6 maanden (HR 0,23), HRD populatie: PFS 13,6 maanden (HR 0,32).
Op basis van de resultaten van de ARIEL 3 studie heeft de CieBOM voor alle patiëntengroepen een positief advies verleend (CieBOM september 2019) 1. Hierdoor is Rubraca toepasbaar voor alle patiënten ongeacht de aanwezigheid van een genetische marker. Interessant om te vermelden, in de ARIEL 3 geïncludeerde patiëntengroepen zaten patiënten met een restziekte (tot aan bulky disease van > 2cm). Rubraca verbeterd de PFS versus placebo bij patiënten met bulky disease ongeacht mutatiestatus met een vermindering van het risico op een recidief van 60% (HR: 0,40).
Daarnaast werden er substantiële verbeteringen gezien in de Rubraca behandelde patiëntengroep die voor een deel van een partiële naar een complete respons gingen in vergelijking met de placebo behandelde patiëntengroep.
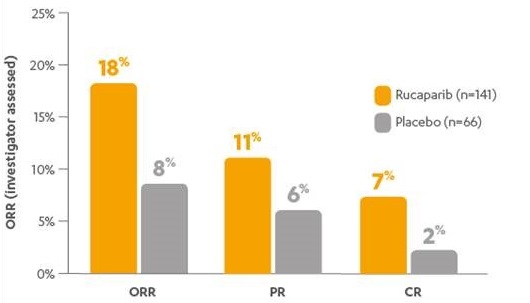
Figuur 1. Response rates van patiënten met meetbare ziekte bij baseline. Bijna 1 op de 5 patiënten hadden een bewezen respons (PR+CR). (ORR: Objective Respons Rate; PR: Partial Response; CR: Complete Response)
Tolerabiliteit was goed hanteerbaar en voornamelijk van voorbijgaande aard. De meest voorkomende graad 3 bijwerkingen waren: anemie 19% en trombocytopenie 5%.
Rubraca biedt een aanvulling in de onderhoudsbehandeling met een bewezen voordeel en met een hanteerbaar bijwerkingenprofiel welke geschikt is voor een brede patiëntengroep.
Rubraca is nu beschikbaar en wordt volledig vergoed (januari 2020- TB/REG-20647-01).
Referenties
1. CieBOM Medische Oncologie sept. 2019
2. Coleman 2017